4.3. Arzt-Patient-Kommunikation
Jörg Dirmaier 1
1 Institut und Poliklinik für Medizinische Psychologie, Universitätsklinikum Hamburg-Eppendorf, Hamburg, Germany
Eine aktive Beteiligung von Patienten und, je nach Situation, auch von Angehörigen wird im Zuge einer zunehmend sich durchsetzenden Patientenorientierung als zentraler Faktor einer qualitativ hochwertigen patientengerechten Kommunikation angesehen. Dies gilt für alle Phasen einer Erkrankung – von der Anamnese, der Diagnosemitteilung und der Aufklärung über Behandlungsmöglichkeiten bis zu einer gemeinsamen medizinischen Entscheidungsfindung sowie der Stärkung der Selbstbeteiligung an der Umsetzung gesundheitsrelevanter Verhaltensänderungen. Diese Entwicklung hin zu einer stärkeren Patientenbeteiligung resultiert aus einem veränderten Rollenverständnis von Patienten in der Arzt-Patient-Beziehung. Ausgehend von einer früher stärker paternalistisch geprägten Arzt-Patient-Beziehung, die den Patienten eine passive Rolle zuschrieb, wollen Patienten heute eine eher aktive, partnerschaftliche bzw. partizipative Rolle im Rahmen der Arzt-Patient-Beziehung einnehmen (zu den unterschiedlichen Beziehungsmodellen s. Kapitel 4.2.). Ein Großteil der Patienten erwartet mittlerweile von ihrem Behandler, über ihre Erkrankung und entsprechende Therapieoptionen umfassend aufgeklärt sowie bei Entscheidungs- und Behandlungsprozessen aktiv beteiligt zu werden [1].
Im folgenden Kapitel werden einerseits Grundlagen der Arzt-Patient-Kommunikation, der Gestaltung der ärztlichen Anamnese, der Informationsvermittlung und der Risikokommunikation im Patientengespräch beschrieben. Andererseits werden die Beteiligung von Patienten an medizinischen Entscheidungen im ärztlichen Gespräch und die Unterstützung dieses Prozesses durch medizinische Entscheidungshilfen erläutert. Schließlich werden kommunikative Strategien zu gesundheitsbezogenen Verhaltensänderungen und zur Steigerung der Gesundheitskompetenz von Patienten erläutert.
4.3.1. Beziehungsaufbau
Ein grundlegender Aspekt einer gelungenen Arzt-Patient-Kommunikation besteht zunächst in der Etablierung einer tragfähigen Arbeitsbeziehung. Das dabei aufgebaute Vertrauen zwischen Arzt und Patient sowie Angehörigen bildet die Grundlage für eine gelingende Anamnese bzw. Diagnosestellung, die individuelle Behandlungsauswahl und weitere Behandlungsplanung. Ein hohes Vertrauen in den Arzt geht mit einer verbesserten therapeutischen Mitarbeit der Patienten (= Adhärenz), höherer Zufriedenheit mit dem Arzt und verbesserter Kontinuität der Behandlung einher. Patienten, die ihrem Arzt vertrauen, berichten z.B. von einem vorteilhafteren Gesundheitsverhalten, weniger Symptomen, einer höheren Lebensqualität und von mehr Zufriedenheit mit der Behandlung. Ebenso kann eine vertrauensvolle Arzt-Patient-Kommunikation zu einer besseren Mitarbeit der Patienten bzw. einer stärkeren Adhärenz bzgl. der gesundheitsbezogenen Maßnahmen bei chronischen oder psychischen Erkrankungen führen, z.B. durch das Einhalten von Ernährungsmaßnahmen oder regelmäßige Insulininjektionen bei Diabetes mellitus.
Die Entstehung von Vertrauen beim Patienten gegenüber dem Arzt wird entscheidend durch das ärztliche Verhalten bestimmt. Interpersonelle und kommunikative Fähigkeiten, wie aktives Zuhören oder das an das Wissen des Patienten angepasste Beantworten von Fragen, begünstigen den Aufbau von Vertrauen. Zudem fördert die aktive Beteiligung von Patienten bei der medizinischen Entscheidungsfindung über das weitere diagnostische und therapeutische Vorgehen das Vertrauen in den Arzt. Eine positive Arbeitsbeziehung ist förderlich für einen von Kooperation und Offenheit geprägten weiteren Gesprächsablauf und wirkt sich nachhaltig auf alle folgenden Aspekte einer Arzt-Patient-Kommunikation aus.
Der Aufbau einer tragfähigen Arbeitsbeziehung erfolgt nicht nur zu Beginn, sondern kontinuierlich über den gesamten Kommunikationsprozess im ärztlichen Gespräch, verläuft also parallel zu anderen Kommunikationsbausteinen, wie der systematischen Informationssammlung bzw. Anamnese, der Anbahnung der Behandlungsentscheidung oder der Planung weiterer Behandlungsschritte [2]. Wird der Beziehungsaufbau vernachlässigt, kann dies die genannten Komponenten der Arzt-Patient-Kommunikation (Adhärenz, Zusammenarbeit, Zufriedenheit) ungünstig beeinflussen. Dies kommt insbesondere dann negativ zum Tragen, wenn sich die Interaktion über mehrere Konsultationen bzw. einen längeren Zeitraum hinweg gestaltet, was bei vielen chronischen Erkrankungen typisch ist.
Wichtig für einen gelungenen Beziehungsaufbau ist insbesondere eine patientenzentrierte Gesprächsführung (vgl. Kapitel 4.2.), wobei diese sowohl verbale als auch non-verbale Aspekte beinhaltet (vgl. Kapitel 4.1.). Es ist einerseits wichtig, die verschiedenen und vielfältigen non-verbalen Ausdrucksweisen auf Seiten der Patienten zu erfassen und adäquat darauf zu reagieren (z.B. das Ansprechen von non-verbal geäußerten Gefühlen). Um Emotionen von Patienten angemessen aufzugreifen und darauf reagieren zu können, kann das sogenannte NURSE-Schema genutzt werden [3]. Dieses beinhaltet fünf kommunikative Strategien, um emotionale Reaktionen auf Seiten der Patienten adäquat aufgreifen zu können:
- (N): Emotionen benennen und ansprechen (naming): „Es hört sich so an, als wären Sie besorgt, dass Ihre Erkrankung wiederkehren könnte.“
- (U): Emotionen verstehen und Verständnis vermitteln (understanding): „So wie ich Sie verstehe, sind Sie besorgt über die Nebenwirkungen des Medikaments.“
- (R): Anerkennung, Respekt zeigen (respecting): „Ich bin beeindruckt, wie gut Sie Ihre Kinder während dieser langen Krankheit weiter betreut haben.“
- (S): Unterstützung anbieten (supporting): „Ich unterstütze Sie gerne während dieser Erkrankung.“
- (E): Emotionen ergründen (exploring): „Warum genau haben Sie diese Befürchtungen?“
Andererseits ist auch das non-verbale Verhalten des Behandlers für einen gelungenen Beziehungsaufbau maßgeblich. Es beinhaltet u.a. Augenkontakt, eine zugewandte Körperhaltung und weitere eindeutige Signale, die das Interesse an den Beschwerden und Themen des Patienten dokumentieren. Darüber hinaus ist eine patientenzentrierte Gesprächsführung gekennzeichnet durch ein hohes Maß an Akzeptanz der von Seiten der Patienten geäußerten Ansichten und Gefühle, durch Empathie, das Anbieten von Unterstützung sowie einen feinfühligen Umgang mit sensiblen persönlichen und gesundheitsbezogenen Themen. Eine mögliche Methode zur Umsetzung einer patientenzentrierten Gesprächsführung stellt die sogenannte Ask-Tell-Ask-Methode dar, welche das Ziel verfolgt, Patienten aktiver in den Kommunikationsprozess mit einzubeziehen. Dabei soll zunächst im Gespräch versucht werden zu verstehen, was Patienten bereits über ihre medizinische Situation wissen und/oder wie ihr emotionaler Zustand ist. Darauf aufbauend können dann die noch benötigten bzw. hilfreichen Informationen vermittelt und erklärt werden. Abschließend sollte sich der Arzt rückversichern, ob die Informationen verstanden wurden und die Bedeutung erfasst wurde.
4.3.2. Anamnese und Informationsvermittlung
4.3.2.1. Anamnese
Die Erhebung einer Anamnese und die Informationssammlung zur Beurteilung der klinischen Situation von Patienten ist eine der wichtigsten und gleichzeitig häufigsten Aufgaben von Ärzten. Unter einer Anamnese wird die professionelle Erfassung bzw. Erfragung von potenziell medizinisch relevanten Informationen verstanden. Dabei antwortet entweder der Patient selbst (Eigenanamnese) oder eine dritte Person (Fremdanamnese). Ziel ist die Erfassung der Krankengeschichte eines Patienten im Rahmen einer aktuellen Erkrankung.
Ein gut durchgeführtes Anamnesegespräch hat mehrere Funktionen: Es dient dem Informationsgewinn für die Diagnosestellung, dem Aufbau einer vertrauensvollen Arzt-Patient-Beziehung und als Basis für eine spätere gemeinsame medizinische Entscheidungsfindung bzgl. zu ergreifender diagnostischer oder therapeutischer Maßnahmen. Wichtig hierbei ist, sich zu vergegenwärtigen, dass eine endgültige Diagnose in der Mehrheit der Fälle, trotz des medizinischen und technologischen Fortschritts, z.B. den Möglichkeiten in der Bildgebung oder bei Laborparametern, insbesondere auf den sorgfältig gesammelten Informationen aus der Anamnese fußt.
Eine Anamnese ist ein interaktiver Prozess, der in Abhängigkeit von der Situation variiert und an die Person des Gegenübers adaptiert werden sollte. Es ergeben sich unterschiedliche anamnestische Herangehensweisen, je nachdem, ob es sich um eine Aufnahmesituation in einer Notfallambulanz einer Klinik (z.B. bei Verdacht auf einen Herzinfarkt), einen ersten Patientenkontakt bei einem Facharzt in einer Praxis nach Überweisung (z.B. zur Abklärung von lange bestehenden Kopfschmerzen) oder den Beginn einer psychotherapeutischen Behandlung (z.B. zur Behandlung einer depressiven Störung) handelt. Die Anamnese kann Fragen z.B. nach subjektiven und vegetativen Beschwerden, nach Vorerkrankungen, familiären Erkrankungen, der Einnahme von Medikamenten, nach bestehenden Risikofaktoren und Ressourcen, nach dem Sexualverhalten und gesundheitsbezogenen Verhaltensweisen (z.B. Ernährung, Bewegung) beinhalten (s. Tabelle 1).
Der Inhalt einer Anamnese entspricht der momentanen Erinnerung des Patienten (oder Angehörigen), der grundsätzliche Ablauf ist häufig gleich. Nach dem Inhalt der Befragung unterscheidet man insbesondere die folgenden Formen, die in ihrer Abfolge, der Tiefe der Inhalte und der Frageformen (offene oder geschlossene Fragen) je nach Bedarf und klinischer Fragestellung variabel gestaltet werden.
|
Anamneseform |
Inhalte |
Beispielfragen |
|
Krankheitsanamnese |
Erhebung des Leitsymptoms/Beschwerden, z.B. zeitliches Auftreten, Lokalisation, Intensität, Begleitsymptomatik, subjektive Krankheitstheorie, ggf. auch frühere Erkrankungen;
Prüfung, ob häufige Erkrankungen vorliegen |
|
|
Vegetative Anamnese |
Körperliche Funktionen, z.B. Allgemeinbefinden, Appetit/Durst, Gewicht/Größe, Fieber, Schlafqualität, Verdauung/Wasser lassen, Husten, Unverträglichkeiten |
|
|
Psychosoziale Anamnese |
Insbesondere psychische Befindlichkeit, Herkunft (Nationalität), Lebenssituation: Versorgungs- und Wohnsituation, Bildung, Beruf, Arbeitssituation, existenzielle Probleme, Belastungen und Ressourcen |
|
|
Medikamentenanamnese
|
Aktuelle, eingenommene Medikamente inklusive Dosierung, Verträglichkeit, frühere Einnahmen und Wirksamkeit, Adhärenz |
|
|
Anamnese zu Lebensstil und Risikoverhalten
|
Ernährungsgewohnheiten, Diäten, Gesundheitsverhalten (z.B. Bewegung), Suchtverhalten, Nutzung von Hilfsangeboten, Reiseanamnese
|
|
|
Familienanamnese |
Betroffenheit von Familienmitgliedern von der aktuellen oder einer verwandten Erkrankung,
Häufung von bestimmten Erkrankungen in der Familie |
|
|
Biografische Anamnese |
Lebensgeschichte des Patienten, v.a. im Kontext von psychotherapeutischen Behandlungen, z.B. psychische Entwicklung, emotionales Klima, in dem der Patient aufgewachsen ist, Leistungen und Erwartungen in der Schule |
|
|
Sexualanamnese
|
Im Vordergrund stehen die Symptomatik und der Hintergrund sexueller Beschwerden und Funktionsstörungen, z.B. Menarche und Zyklusanamnese, Potenz und Orgasmusfähigkeit, sexuelle Gewohnheiten, Veränderungen sexueller Empfindungen |
|
4.3.2.2. Aufklärung und Diagnosemitteilung
Über Epochen haben Ärzte medizinische Entscheidungen im Interesse ihrer Patienten getroffen, um deren Wohl oder Gesundheit zu steigern, ohne jedoch ihre volle Zustimmung eingeholt zu haben. Dieses früher übliche Vorgehen stößt heute aufgrund der gestärkten Patientenautonomie und der Wünsche von Patienten nach Information und Beteiligung am medizinischen Entscheidungsprozess an seine Grenzen. Ärzte sind also dem Wohl ihrer Patienten verpflichtet und haben zugleich den Willen des Kranken zu achten. Das juristisch gültige Selbstbestimmungsrecht von Patienten wird insbesondere durch die ärztliche Pflicht zur Aufklärung gewährleistet. Unter ärztlicher Aufklärung werden in diesem Zusammenhang die Information eines Patienten über seine Erkrankung sowie die geplanten Diagnostik- und Therapiemaßnahmen im Rahmen der medizinischen Heilbehandlung verstanden. Diese Informationsweitergabe stellt eine zentrale Vorbedingung für das sogenannte informierte Einverständnis des Patienten (engl. informed consent) dar, also die Zustimmung zu medizinischen Maßnahmen, die im Rahmen der Behandlung durchgeführt werden sollen. Es gelten folgende Grundsätze:
- Patienten müssen prinzipiell in die jeweilige konkrete Diagnose- oder Behandlungsmaßnahme einwilligen.
- Die ärztliche Aufklärungspflicht bezieht sich nicht nur auf das Ob, sondern auch auf die Art und Weise der medizinischen Maßnahme: Patienten bleibt überlassen, ob sie sich behandeln lassen wollen und für welche Risiken und Chancen alternativ zur Verfügung stehender Therapien sie sich entscheiden.
- Der behandelnde Arzt hat die wesentlichen Grundlagen für diese von Patienten zu treffende Entscheidung zu vermitteln. Dies wahrt die Freiheit und Würde der Person.
Die ärztliche Aufklärung lässt sich nicht an andere Berufsgruppen delegieren. Gleichwohl können andere Heilberufe in den Prozess der Aufklärung miteinbezogen werden bzw. über den Stand der Aufklärung informiert sein. So können z.B. geschulte Pflegekräfte die medizinische Entscheidungsfindung mittels des Einsatzes von Gesundheitsinformationen bzw. von Entscheidungshilfen (s. Abschnitt 4.3.3.3.) unterstützen (sogenannte Decision Coaches). Die Aufklärung besteht in der Regel nicht aus einem einzigen Gespräch, sondern ist als ein kommunikativer Prozess zu sehen, der das Arzt-Patient-Verhältnis begleitet. Dies gilt vor allem für die Übermittlung von Gesundheitsinformationen, ärztlichen Diagnosen und Therapievorschlägen, für deren Verarbeitung Patienten Zeit benötigen, z.B. vor der Behandlung einer Krebserkrankung mit Operation, Chemo- und Strahlentherapie oder der medikamentösen und psychotherapeutischen Behandlung einer Essstörung.
Seit 2013 ist das Behandlungs- und Arzthaftungsrecht im Bürgerlichen Gesetzbuch mit dem Gesetz zur Verbesserung der Rechte von Patientinnen und Patienten (Bundesgesetzblatt 2013, [4]) neu geregelt. Ziel war es, für alle Beteiligten im Gesundheitswesen, Ärzte und andere Gesundheitsberufe, Patienten sowie Angehörige, Transparenz über das geltende Recht herzustellen. Die Regelungen beziehen sich einerseits auf die Grundlagen des Behandlungsvertrages (= zivilrechtlicher Vertrag zwischen dem Behandelnden und dem Patienten über die entgeltliche Durchführung einer medizinischen Behandlung [5] und bündeln andererseits die Patientenrechte im Falle eines möglichen Behandlungsfehlers. Hierunter wird ein den Patienten schädigendes ärztliches Verhalten bei einer medizinischen Behandlung verstanden, welches den aktuellen Kenntnisstand der medizinischen Wissenschaft zum Behandlungszeitpunkt missachtet und damit die notwendige Sorgfalt und Vorgehensweise nicht ausreichend wahrt.
4.3.2.3. Aufklärungsformen und Informationsvermittlung
Unter Diagnoseaufklärung wird das Informieren des Patienten über die medizinischen Befunde verstanden (insbesondere, dass er krank ist und an welcher Krankheit er leidet). Die Verlaufsaufklärung erstreckt sich auf Art, Umfang und Durchführung von Eingriffen bzw. medizinischen Maßnahmen. Die Risikoaufklärung vermittelt Patienten Informationen über die möglichen Gefahren eines ärztlichen Eingriffs (z.B. Nachblutung nach einem operativen Eingriff). Diese Aufklärungspflicht lautet wörtlich im Patientenrechtegesetz nach § 630e BGB [4]:
Jeder medizinische Eingriff in den menschlichen Körper erfüllt juristisch den objektiven Tatbestand der Körperverletzung. Der Eingriff bedarf deshalb der Einwilligung des Patienten, um gerechtfertigt und damit nicht strafbar zu sein. Entsprechend soll eine ärztliche Aufklärung mündlich, persönlich und rechtzeitig vor einem Eingriff bzw. einer Maßnahme erfolgen, damit Patienten über Entscheidungen ausreichend nachdenken können. Ausnahmen sind beispielsweise unaufschiebbare Operationen oder eine lebensrettende Erstversorgung nach einem Unfall, wenn die Einwilligung des Patienten angenommen werden kann. Weiterhin soll die Aufklärung für den Patienten verständlich sein und dem Patienten werden Unterlagen, die er im Zusammenhang mit der Aufklärung oder Einwilligung unterzeichnet hat, ausgehändigt (z.B. die schriftliche Einwilligung zur Operation). Darüber hinaus sollte die Aufklärung in geeigneter Form vom Arzt selbst dokumentiert werden (z.B. in der elektronischen Patientendokumentation oder Krankenakte).
Eine gelungene Informationsvermittlung ist eng mit einer effektiven kognitiven Verarbeitung verknüpft, v.a. Prozessen wie Erinnern und Verstehen, die durch Faktoren wie Stress (wegen einer Erkrankung) oder intensive Emotionen (z.B. Angst vor einer schweren Diagnose) negativ beeinflusst werden kann (s. hierzu auch Kapitel 2.1. und Kapitel 2.2.). Auch deswegen sollen Informationen von Seiten des Behandlers so strukturiert und vermittelt werden, dass sie vom Patienten verstanden und vom Arbeits- in das Langzeitgedächtnis transferiert werden können. Bei der Informationsvermittlung ist zu beachten, dass Patienten sehr unterschiedliche medizinische Informations- und Wissensstände, unterschiedliche Bildungs- und Sprachniveaus sowie differierende Informationswünsche haben. Diese Aspekte werden heute unter dem Begriff der Gesundheitskompetenz (health literacy) zusammengefasst, die es einerseits zu beachten, andererseits zu fördern gilt (s. Abschnitt 4.3.5.). Weitere Variablen wie die Glaubwürdigkeit der Quelle (Behandler), die Art der Information (spezifisch vs. allgemein), die Art und Weise der Informationsvermittlung (z.B. Wiederholung, Nutzung verschiedener Kommunikationskanäle) und die Bewertung der Information auf Seiten des Patienten (positiv vs. negativ) beeinflussen das Verstehen und Erinnern von Gesundheitsinformationen. Dementsprechend ist das Ziel einer gelungenen Informationsvermittlung also nicht nur, Patienten relevante Informationen über Erkrankung und Behandlung zur Verfügung zu stellen, sondern auch sicherzustellen, dass diese Informationen verstanden und erinnert werden, um sie später bei der medizinischen Entscheidungsfindung nutzen zu können. Das „Vier-Seiten-Modell“ von Friedemann Schulz von Thun ([6], S. 268) verdeutlicht, dass Informationen bzw. Nachrichten sowohl vom Sender als auch vom Empfänger nach den vier Aspekten Sachinhalt, Selbstoffenbarung, Beziehung und Appell interpretiert werden können (vgl. Kapitel 4.1.). Diese Aspekte sind in der ärztlichen Kommunikation von großer Bedeutung, da dort meist davon ausgegangen wird, dass nur Informationen als Sachinhalt vermittelt werden. Hier wird häufig vernachlässigt, dass die Informationsverarbeitung mindestens ebenso sehr von den anderen Aspekten beeinflusst wird. So kann die Aussage „Ich habe immer noch starke Schmerzen“ im ärztlichen Gespräch neben der Information, dass Schmerzen vorhanden sind (Sachinhalt), auch eine Enttäuschung über das bisher erzielte Behandlungsergebnis (Selbstoffenbarung), die Zuweisung der Rolle als Behandler/Arzt (Beziehung), sowie die Bitte um Hilfe (Appell) beinhalten.
4.3.2.4. Besondere Aufklärungssituationen
Gespräche mit schwerkranken und sterbenden Patienten und die Mitteilung von ernsten Diagnosen stellen besondere Anforderungen dar und gehören für Ärzte häufig zu den als schwierig erlebten Situationen ihrer Berufsausübung.
Heute ist Bestandteil der ärztlichen Aufklärungspflicht, Patienten so weit wie möglich über ihre Krankheit und die notwendigen Maßnahmen zu informieren, wobei sich die Informationsgabe an den Informationsbedürfnissen und dem Beteiligungswunsch der Patienten orientieren soll [7]. Bei dieser prinzipiell richtigen und angemessenen Strategie, Patienten umfassend aufzuklären, gilt es zu bedenken, dass eine Minderheit von Patienten nicht vollständig über die Krankheit und therapeutische Maßnahmen informiert werden will oder spezifische Bewältigungsstrategien, zum Beispiel Verleugnung, nutzt, um starke emotionale Belastungen durch die Information über eine schwere Erkrankung und die daraus sich ergebenden Behandlungen (zunächst) zu vermindern (vgl. Represser vs. Sensitizer, Kapitel 2.3. und Kapitel 3.2.1.). Es kann auch vorkommen, dass Patienten aus anderen Kulturkreisen bzw. mit anderer Einstellung zur Arzt-Patient-Beziehung hiervon Gebrauch machen. Patienten können und dürfen zudem auf Aufklärung verzichten und sich ganz ihrem Arzt anvertrauen. Dieses Wissen ist für Ärzte von hoher Bedeutung, um diese Patienten in den Aufklärungs- und Informationsgesprächen nicht zu überfordern. Hier muss folglich eine gute Balance zwischen der ärztlichen Aufklärungspflicht und dem Informationswunsch des Patienten gefunden werden, z.B. indem – wenn möglich – Zeit für diese Prozesse eingeräumt wird. In jedem Fall sollte das Informationsbedürfnis der Patienten frühzeitig abgeklärt und immer wieder hinterfragt werden. Wenn primär Sprachbarrieren eine Einschränkung bei der Informationsvermittlung darstellen, spielen Dolmetscher eine immer größere Rolle. Nicht-professionelle Dolmetscher sind häufig Personen aus dem gleichen Land oder Sprachraum (z.B. Mitarbeiter medizinischer Einrichtungen oder Familienangehörige), professionelle Dolmetscher verfügen über die notwendigen Sprachkenntnisse und über die erforderlichen medizinischen Fachkenntnisse.
Aufzuklären ist üblicherweise der einsichtsfähige Patient, d.h. der Patient muss in der Lage sein, Anlass, Wesen, Bedeutung und Tragweite sowie das Für und Wider der beabsichtigten medizinischen Maßnahme in den Grundzügen zu erfassen, in die er einwilligen soll. Die Aufklärung soll aufzeigen, was der Eingriff bzw. die vorgeschlagene Maßnahme für die persönliche Situation des Patienten bedeuten kann. Folglich kommt es rechtlich primär auf die Einsichtsfähigkeit und nicht auf die Geschäftsfähigkeit an. Hält ein Arzt einen Patienten für nicht einwilligungsfähig und hat dieser keine sogenannte Vorsorgevollmacht1 zugunsten eines Dritten erteilt, muss üblicherweise ein Betreuer bestellt werden, der die medizinische Entscheidung für den Patienten dann treffen kann.
4.3.2.5. Psychologische Aspekte der Aufklärungssituation
Patienten, insbesondere schwer und chronisch Erkrankte, erwarten und benötigen (in der Regel, s.o.) eine umfassende Aufklärung über ihre Erkrankung und die bestehenden therapeutischen Möglichkeiten. Aufklärung dient der Orientierung, der Reduktion von Ängsten und fördert eine dem Patienten Sicherheit gebende Arzt-Patient-Beziehung. Für die Aufklärung wurden Praxisempfehlungen formuliert, die eine schrittweise Informationsvermittlung im Dialog, orientiert an der Aufnahmebereitschaft des Patienten, vorschlagen (z.B. [8]).
Zu fragen ist, ob der Patient überhaupt Genaueres über Diagnose und Prognose wissen möchte: „Möchten Sie, dass ich Ihnen mitteile, wie die Krankheit bei den meisten Patienten mit gleicher Diagnose verläuft?“ |
Um einen Anknüpfungspunkt für das Aufklärungsgespräch zu erhalten, ist es sinnvoll, den Patienten nach seinem aktuellen Wissensstand zu befragen: „Bevor ich Ihnen sage, was bei der Untersuchung herausgekommen ist, würde ich gerne wissen, was man Ihnen bisher schon mitgeteilt hat. Dann weiß ich besser, womit ich anfangen soll.“ |
Hiermit ist die einfache und ehrliche Informationsmitteilung unter Benutzung von Alltagssprache gemeint, ggf. unter Nutzung unterschiedlicher Medien, zum Beispiel Grafiken. |
Hier wird in einfachen Worten nachgefragt, ob der Patient alle Informationen verstanden hat, die mitgeteilt wurden: „Können Sie die von mir übermittelten Informationen noch einmal in eigenen Worten zusammenfassen, damit ich sehe, was bei Ihnen angekommen ist?“ |
Nach jeder Information wird kurz innegehalten, damit der Patient nachfragen kann oder ermutigt wird, nachzufragen. |
Bei der Prognosemitteilung sollten üblicherweise keine konkreten Zeiten genannt werden, da dies im Einzelfall unmöglich ist, sondern ein breiter, realistischer Zeitrahmen vermittelt werden, der dem Patienten ermöglicht, die persönlichen Angelegenheiten zu regeln. |
Dem Patienten wird verständlich dargelegt, dass er nach ausreichender Informationsvermittlung die Möglichkeit hat, sich an der Entscheidung über die Behandlung beteiligen zu können. Dabei sollte abgeklärt werden, ob der Patient diese Möglichkeit in Anspruch nehmen möchte. |
Insbesondere bei Krebserkrankungen sollten zuerst die Heilungschancen und erst danach die Wahrscheinlichkeit eines Rückfalls angesprochen werden. Bei der palliativen Behandlung, die als Ziel die Linderung der Symptome einer Erkrankung hat, Äußerungen vermeiden wie, „dass nichts mehr getan werden kann“. Stattdessen sollte vermittelt werden, dass alles getan wird, um eine möglichst gute Lebensqualität aufrechtzuerhalten. |
Dem Patienten sollte nur so viel Information auf einmal vermittelt werden, wie er intellektuell und emotional verarbeiten kann. Ihm sollte ermöglicht werden, Nachfragen zu stellen und auch das Gespräch zu beenden, falls er sich überfordert fühlt, noch weitere Informationen aufzunehmen. |
Wichtig ist, den Patienten zu ermutigen, Gefühle zu äußern. (Starke) Gefühle sind normal in kritischen Aufklärungssituationen, hier kann auch über psychosoziale Unterstützungsmöglichkeiten informiert werden. |
Informationsvermittlung ist kein Alles-oder-Nichts-Phänomen, sondern braucht Zeit zur gedanklichen und emotionalen Verarbeitung. Termine für eine Nachbesprechung sollten vorgeschlagen werden, ggf. gemeinsam mit einem Angehörigen. |
Aufklärung von Patienten besitzt darüber hinaus besondere Bedeutung im Zusammenhang mit der Übermittlung ungünstiger Nachrichten. Gemäß Langewitz [9] sollte der Überbringer ernster Nachrichten :
- sich bezüglich der zu übermittelnden Information sorgfältig vorbereiten;
- prüfen, ob eine dritte Person (z.B. Pflegekraft, Angehöriger) anwesend sein sollte;
- eine ruhige Umgebung suchen, in der eine ungestörte Atmosphäre gewährleistet ist;
- ungünstige Nachrichten mit einem ausreichenden Zeitpolster übermitteln.
Ein schwer erkrankter Patient benötigt ausreichend Zeit, um sich mit einer ungünstigen Diagnose auseinandersetzen zu können. Bei der ersten Konfrontation von Patienten werden häufig bedrohlich wirkende Bilder und Vorstellungen über schwerwiegende Krankheiten aktiviert. Die kognitiven Fähigkeiten sind in diesen Situationen oft eingeschränkt und der Betroffene kann weitreichende Informationen nur begrenzt aufnehmen und verarbeiten. Psychische Verarbeitung von schwerwiegenden Aufklärungsinhalten vollzieht sich in der Regel in unterschiedlichen Phasen und wird von mehr oder weniger starken Emotionen begleitet: Gefühle und Reaktionen wie Aggression und Anklage, Hilfesuche, Nicht-Wahrhaben-Wollen, Zuversicht oder Depression können sich im raschen Wechsel einstellen. Subjektive Krankheitstheorien bzw. Laientheorien (vgl. Kapitel 3.2.1.) über die Verursachung der Erkrankung (z.B. Schuldgefühle, weil sich Patienten selbst zu viel „Stress“ zugemutet haben und glauben, deswegen erkrankt zu sein) können zur Aktualisierung von unterschiedlichen Gefühlen führen. Solche Erklärungsversuche sind meist im Kontext der spezifischen Lebensgeschichte der Patienten zu sehen, wobei diese Vorstellungen potentiell als zusätzliche Belastung erlebt werden können, v.a. wenn sie sich auf mögliche eigene „Fehler“ etc. beziehen. Daher sollten die subjektiven Krankheitsvorstellungen in dieser Phase oder bereits bei der Anamnese (s. Tabelle 1) thematisiert werden.
Worüber aufzuklären ist, wird vor allem durch die jeweilige Situation bestimmt (zum Beispiel Diagnose, Prognose, Therapie oder Verlaufskontrolle, stationäre oder ambulante Behandlung, Nachsorge, kindliche, jugendliche oder erwachsene Patienten, psychosoziale Situation des Patienten usw.). Wiesing, Bürger et al. [10] zufolge, sind wichtige inhaltliche Aspekte u.a. die folgenden:
- Kurze Zusammenfassung der Befunde, die zur Diagnose geführt haben;
- Nennung der genauen Diagnose in einer für den Patienten verständlichen Form;
- Beschreibung der Art der Erkrankung und des momentanen Stadiums;
- Beschreibung des natürlichen Verlaufs der Erkrankung;
- Information über verschiedene Therapiemöglichkeiten unter Formulierung möglicher Therapieziele (z.B. Heilung, Lebensverlängerung, Linderung von Beschwerden);
- Aufklärung über Therapieverfahren, insbesondere über gleichwertige Therapiealternativen unter Nennung des normalen, unkomplizierten Ablaufs einer Therapie;
- Information über Risiken sowie somatische und mögliche psychische Nebenwirkungen;
- Einschätzung der Prognose und Angebot an Patienten, weitere Fragen zu stellen.
Obwohl das ärztliche Aufklärungsgespräch nicht an andere Berufsgruppen delegiert werden darf, ist eine enge Kooperation innerhalb des therapeutischen Teams dennoch unbedingt erforderlich, da Patienten, die durch die Art ihrer Erkrankung in eine existentielle Krisensituation geraten, sich mit ihren Fragen und Sorgen häufig an Pflegekräfte oder weitere Gesundheitsberufe wenden. Diese können damit eine Vermittlerrolle zwischen Arzt, Patient und Angehörigen übernehmen.
Entsprechende Aus- und Weiterbildungsprogramme zur Vorbereitung von Studierenden und Ärzten auf die Diagnosemitteilung und Aufklärung bei schwierigen medizinischen Situationen wurden im Rahmen spezifischer Kommunikationstrainings, insbesondere für den onkologischen Bereich, entwickelt und evaluiert. Bekannt ist in diesem Zusammenhang das sechsstufige SPIKES-Protokoll [11]. Die Ziele umfassen zunächst das Sammeln von Informationen über den aktuellen Wissensstand des Patienten und das Mitteilen der medizinischen Fakten in Abhängigkeit von den Patientenbedürfnissen. Weiterhin wird von Seiten des Arztes Unterstützung signalisiert und ein Behandlungsplan entwickelt.
|
Schritte |
Vorbereitung und Fragen
|
|
S – Setting up the interview |
|
|
P – Assessing the patient's perception
Offene Fragen, zur Einschätzung der Patientenwahrnehmung |
|
|
I – Obtaining the patient's invitation
Einschätzen der Bereitschaft, die ungünstige Nachricht aufzunehmen |
|
|
K – Giving knowledge and information to the patient
|
|
|
E – Addressing the patient's emotions with empathic responses
Empathische Äußerungen signalisieren Unterstützung. |
|
|
S – Strategy and summary
Abhängig vom Befinden des Patienten wird das weitere Vorgehen ausführlich besprochen. |
|
4.3.2.6. Risikokommunikation
Die Kommunikation von Risiken umfasst die Risikowahrnehmung, die Risikoberatung bis hin zur Risikoprävention mit dem Ziel, Fehlurteile bzw. -entscheidungen in der Medizin zu verringern. Eine professionelle ärztliche Risikokommunikation ist eine wichtige Voraussetzung dafür, dass Patienten die Bedeutung von medizinischen Befunden (z.B. von Vorsorgeuntersuchungen für die Primär- oder Sekundärprävention) oder die Erfolgschancen von Behandlungsmaßnahmen (z.B. für die Abwägung, ob sie die Maßnahme in Anspruch nehmen wollen oder nicht) verstehen und informiert entscheiden können, welche diagnostischen und therapeutischen Maßnahmen für sie angemessen sind. Ein Risiko wird im Folgenden als statistische Unsicherheit verstanden, welches sich auf Basis von empirischen Fakten in Zahlen ausdrücken lässt. Subjektive Wahrscheinlichkeiten (oder auch der subjektive Überzeugungsgrad) von Ereignissen oder der Wirksamkeit von Behandlungsmaßnahmen werden durch die Interpretation empirischer Fakten gebildet. Zum Beispiel kann ein Behandler aufgrund seiner Praxiserfahrung die Überlebenschance eines Patienten als Wahrscheinlichkeit im Sinne einer Prozentangabe ausdrücken: „70% der Patienten, die mit Ihrem Erkrankungsbild zu mir in die Praxis kommen, überleben.“ Das hilft individuellen Patienten allerdings nur bedingt weiter. Zum einen versteht nicht jeder, was der Ausdruck ‚70%‘ wirklich bedeutet, nämlich 7 von 10 oder 70 von 100. Selbst wenn sie das aber verstehen, fehlt ihnen zum anderen eine Information, was dies für den Einzelfall bedeutet, also ob sie der Teilgruppe von Patienten angehören, die eine gute Überlebenschance hat oder nicht.
Die Bedeutung dieses Perspektivwechsels wird besonders deutlich, wenn es um die Ergebnisse von diagnostischen Untersuchungen geht und darum, wie sicher diese Ergebnisse sind. Aus Sicht eines Testentwicklers ist es wichtig zu wissen, wie viel Prozent der getesteten Personen vom Test richtig eingeordnet werden, also
- wie viel Prozent der erkrankten Personen auch tatsächlich positiv getestet werden (die Sensitivität bezeichnet den Anteil der erkrankten Personen, auf die dies zutrifft), bzw.
- wie viel Prozent der gesunden Personen auch tatsächlich negativ getestet werden (die Spezifität bezeichnet den Anteil der Gesunden, auf die dies zutrifft).
Dagegen interessiert den Patienten (und den behandelnden Arzt), ob seine individuelle Diagnose richtig ist, also
- wie hoch die Wahrscheinlichkeit ist, dass die bei ihm gerade diagnostizierte Erkrankung auch tatsächlich vorliegt. Der positive Vorhersagewert (oder auch die positive Korrektheit) bezeichnet genau diese Wahrscheinlichkeit, bzw.
- wie hoch die Wahrscheinlichkeit ist, dass die gegebene Entwarnung („Sie haben die Krankheit nicht“) tatsächlich gerechtfertigt ist. Der negative Vorhersagewert (synonym: negative Korrektheit) bezeichnet den Anteil der negativ getesteten Personen, auf die dies zutrifft.
Diese Überlegungen verdeutlichen, dass es auch falsche Testergebnisse gibt, also solche, die die Person als krank einstufen, obwohl die Erkrankung nicht vorhanden ist (falsch positiv), oder solche, die die Person nicht als krank diagnostizieren, obwohl die Erkrankung vorhanden ist (falsch negativ).
Sensitivität, Spezifität sowie positiver und negativer Vorhersagewert sind folglich Kriterien, die die Güte eines diagnostischen Tests wiedergeben. Dabei ist zu beachten, dass Sensitivität und Spezifität von der Prävalenz, also der Häufigkeit einer Erkrankung, unabhängige Größen sind, wohingegen die Vorhersagewerte durch die Prävalenz beeinflusst werden.
Beispiel:
Angenommen, es sind z.B. von 100 Personen 10 mit einem Virus infiziert, dann beschreibt die Sensitivität eines Tests, wie viele tatsächlich als mit dem Virus infiziert erkannt werden. Liegt z.B. die Sensitivität eines Tests bei 90%, werden von den 10 infizierten Personen 9 erkannt, eine bleibt unentdeckt. Die Spezifität stellt dagegen dar, wie viele der tatsächlich nicht mit dem Virus belasteten Personen auch als solche erkannt werden. Liegt die Spezifität des Tests z.B. bei 80%, werden 72 von den 90 nicht mit dem Virus infizierte Personen korrekt erkannt, bei 8 wird der Virus nachgewiesen, obwohl dieser nicht vorhanden ist. Insgesamt kommt es in diesem Beispiel bei 100 Personen zu 17 positiven Diagnosen („Sie haben die Krankheit“) von denen aber nur 9 richtig sind. Der positive Vorhersagewert beträgt damit nur 9/17=0,53 oder 53% (s. Abbildung 1).
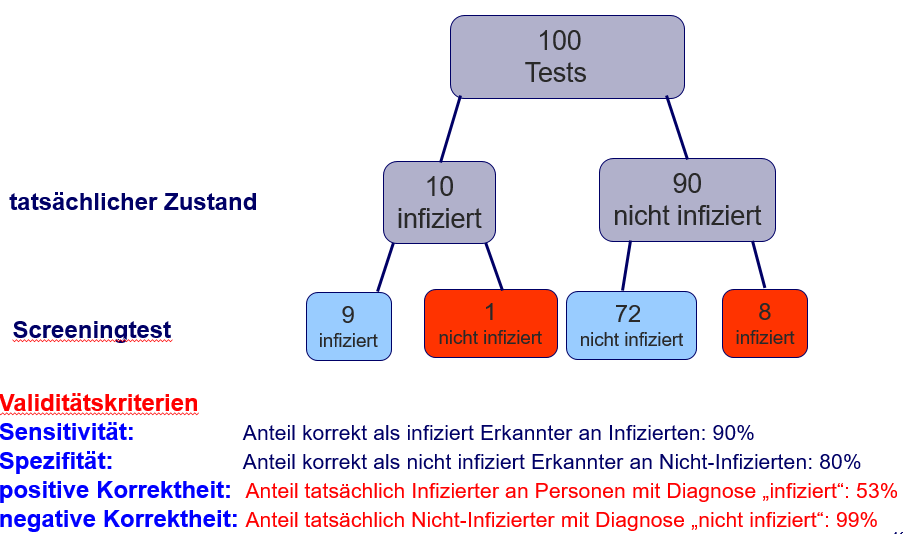
Aufgabe 1:
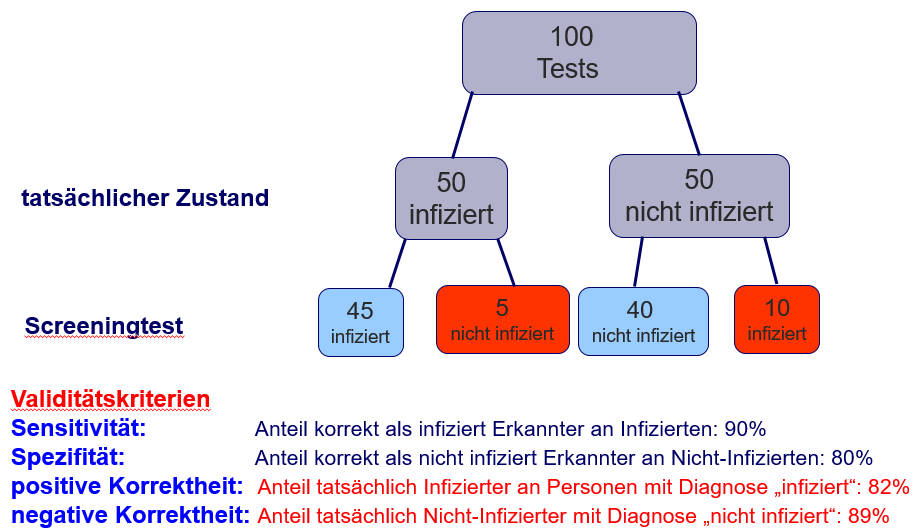
Berechnen Sie die positive Korrektheit desselben Tests, für den Fall, dass von 100 Personen 50 mit dem Virus infiziert sind! Welchen Einfluss hat also die Prävalenz einer Erkrankung auf die positive Korrektheit eines diagnostischen Verfahrens?
(Die Lösung finden Sie am Ende des Abschnitts 4.3.2.6.)
Gesundheitsbezogene Risikoangaben dienen dazu, dass sowohl Laien bzw. Patienten als auch Ärzte und andere Gesundheitsberufe den Nutzen beziehungsweise die Vor- und Nachteile einer medizinischen Leistung, wie beispielsweise einer diagnostischen Maßnahme oder eines Medikaments, mit Hilfe der vorliegenden empirischen Daten besser abwägen können. Häufigkeitsbasierte Risiken werden unterschiedlich dargestellt:
- Einzelfallwahrscheinlichkeiten erklären, mit welcher Wahrscheinlichkeit ein bestimmtes Ereignis auftritt. Z.B. erklärt ein Arzt dem Patienten, dass die Behandlung durch ein bestimmtes Medikament zu 90% eine Linderung seiner Symptome erbringen würde. Problem ist jedoch, dass er keinen Bezug bzw. keine Bezugsklasse benennt, auf welche sich diese Einzelwahrscheinlichkeit bezieht. So kann es sein, dass der Arzt meint, dass 90% der Patienten, die in wissenschaftlichen Studien mit diesem Medikament behandelt wurden, eine Linderung erfahren haben, der Patient aber versteht, dass seine Symptome um 90% unter dem Medikament geringer werden würden.
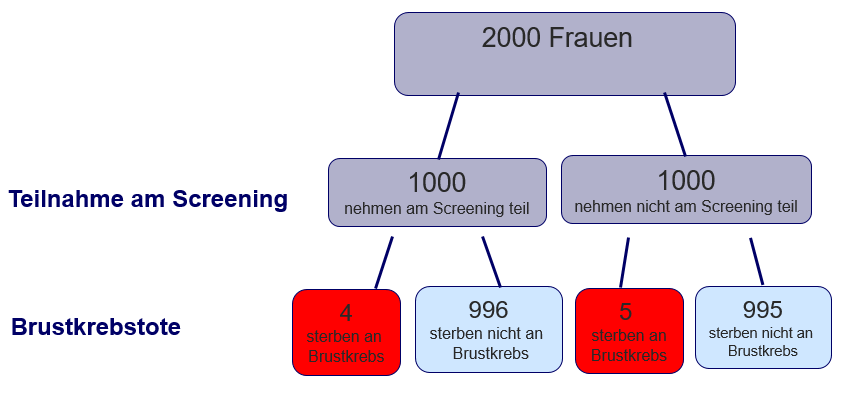
- Bedingte Wahrscheinlichkeiten beschreiben, wie wahrscheinlich es ist, dass ein Ereignis A eintritt, wenn Ereignis B gegeben ist. So tritt z.B. Ereignis A, ein positives Brustkrebsscreening, ein, wenn B, die Frau hat tatsächlich Brustkrebs, gegeben ist. Bedingte Wahrscheinlichkeiten werden häufig in Informationsbroschüren für Patienten genutzt. Studien konnten jedoch zeigen, dass diese Darstellung ebenfalls eine hohe Rate an Missverständnissen mit sich bringt. Z.B. beträgt die Wahrscheinlichkeit 1%, dass eine Frau bei einem MammographieScreening Brustkrebs hat; diese an Brustkrebs erkrankte Frau wird mit einer 80%igen Wahrscheinlichkeit einen auffälligen Befund haben. Wenn sie jedoch keinen Brustkrebs hat, beträgt die Wahrscheinlichkeit eines auffälligen Befunds 10%. Häufig verwechseln Patienten und Ärzte bei dieser Darstellung die Sensitivität (80%) mit dem positiven Vorhersagewert, der in diesem Zahlenbeispiel nur ca. 7% beträgt (zur Erklärung s. nächster Absatz) [12].
- Absolute Häufigkeiten konnten in Studien im Vergleich zu bedingten Wahrscheinlichkeiten korrekter nachvollzogen werden. So übersetzt würde sich das Beispiel aus dem vorangegangenen Absatz folgendermaßen lesen: „10 von 1.000 Frauen, die am MammographieScreening teilnehmen, haben Brustkrebs; 8 von diesen 10 Frauen erhalten einen auffälligen Befund. Von den restlichen 990 Frauen ohne Brustkrebs erhalten 99 einen auffälligen Befund was bedeutet, dass 8 von 107 Frauen mit auffälligem Befund tatsächlich auch Brustkrebs haben.“ Studien bestätigen, dass die Darstellung von absoluten Häufigkeiten gegenüber bedingten Wahrscheinlichkeiten bei Menschen statistisches Denken sowie das Verstehen erleichtern [12]. Dies liegt einerseits an der Verwendung von ganzen Zahlen im Gegensatz zu Prozenten, andererseits schließen absolute Häufigkeiten automatisch eine Bezugsklasse mit ein. Durch die Angabe absoluter Häufigkeiten wird definiert, wie viele Personen Y aus einer Menge X im Schnitt an einer gewissen Erkrankung leiden.
- In Informationsbroschüren, aber auch wissenschaftlichen Publikationen wird der Nutzen einer Maßnahme oft in Form einer relativen Risikoreduktion dargestellt. Diese Darstellung führt meist dazu, dass der Nutzen einer Maßnahme überschätzt wird. Eine Darstellung als absolute Häufigkeiten oder Number needed to treat (oder to screen) führt hier zu realistischeren Einschätzungen, wie das folgende Beispiel veranschaulicht, dem jeweils dieselben Zahlen zugrunde liegen (die auf tatsächlichen Untersuchungen beruhen und den aktuellen Stand der Wissenschaft reflektieren).
- Relative Risikreduktion (Beispiel): „Das Risiko, an Brustkrebs zu sterben, kann durch eine regelmäßige Teilnahme am Mammographie-Screening um 20% gesenkt werden.“ Viele Betroffene und auch Ärzte glauben bei einer solchen Darstellung, dass 20 von 100 Frauen davon profitieren, wenn sie an dem Screening teilnehmen.
- Abslute Risikoreduktion (Beispiel): „Das Risiko, an Brustkrebs zu sterben, ist bei Frauen, die am Screening teilnehmen, um 0,1% niedriger als bei Frauen, die nicht am Screening teilnehmen.“
- Numbers needed to treat bzw. to screen (Anzahl der notwendigen Behandlungen/Screenings; NNT/NNS): „1.000 Frauen müssen regelmäßig am Screening teilnehmen, um den Tod von einer Frau durch Brustkrebs zu verhindern.“ Diese Kennzahl wird verwendet, um Behandlungsverfahren zu vergleichen. Die NNT gibt die Anzahl von Patienten an, die untersucht oder behandelt werden müssen, um einen Todes- oder Krankheitsfall zu verhindern. Sie entspricht dem Kehrwert der absoluten Risikoreduktion. Wenn statt des Behandlungserfolges die Nebenwirkungen betrachtet werden, wird die Methode auch als Number needed to harm (NNH) bezeichnet.
Aufgabe 2:
Versuchen Sie, einen Baum mit natürlichen Häufigkeiten analog zu Abbildung 1 zu zeichnen, der diese Zahlen graphisch veranschaulicht. Versuchen Sie anhand dieses Baums zu klären, wie sich die Zahlen auf unterschiedliche Entscheidungen auswirken können und welche Konsequenzen sich daraus ergeben können.
(Die Lösung finden Sie am Ende des Abschnitts 4.3.2.6.)Aus diesen Beschreibungen und Beispielen geht hervor, dass eine mehr oder weniger realistische und wahrheitsgetreue Interpretation eines Risikos erreicht wird, je nachdem wie die entsprechenden Zahlen bzw. Wahrscheinlichkeiten oder Risiken dargestellt werden. Die meisten Patienten schätzen Nutzen und Schaden von Behandlungsmöglichkeiten nicht realistisch ein. Die Mehrheit der Patienten überschätzt den Nutzen einer Therapie und unterschätzt den Schaden. Missverständnisse können daher im ärztlichen Gespräch v.a. durch eine verbesserte Risikokommunikation und eine transparente Darstellung von Gesundheitsinformationen sowie ein besseres statistisches Verständnis bei Behandler und Patienten verringert werden. Das Harding Center für Risikokompetenz (https://www.hardingcenter.de) hält für Ärzte und Patienten verschiedene Formen von Risikodarstellungen bereit, die sich in wissenschaftlichen Studien als besonders gut verständlich erwiesen haben (s. Abbildung 2).

Auch Behandler haben selten eine korrekte Einschätzung der Risiken bzw. des Nutzens einer Behandlung, die Ungenauigkeiten gehen jedoch in beide Richtungen: Risiken werden häufiger unterschätzt, Nutzen häufiger überschätzt [14].
- Bei der Darstellung von Zahlen und Risikoangaben in ärztlichen Gesprächen und durch Gesundheitsinformationen sollte auf Folgendes geachtet werden:
- Risiken sollten quantitativ, d.h. durch numerische Darstellungen, ausgedrückt werden (z.B. „20 von 100 Patienten erleiden ein Rezidiv“). Eine allein qualitative Darstellung (z.B. „wenige Patienten erleiden ein Rezidiv“) sollte vermieden werden.
- Für die Vermittlung sollten Zahlenangaben in natürlichen Häufigkeiten (absolute Zahlen, z.B. 5 von 100 Patienten) anstatt Prozentangaben (5% der Patienten) genutzt werden.
- Zur Darstellung von Behandlungsergebnissen kann entweder der Nutzen (z.B. „95 von 100 Patienten überleben“) oder der Schaden (z.B. „5 von 100 Patienten sterben“) betont werden (= framing). Bei der Vermittlung von Gesundheitsinformationen sollte auf ein ausgewogenes Framing geachtet werden, um Patienten nicht in Richtung Nutzen oder Schaden einer Behandlung zu beeinflussen.
- Bei der Darstellung von Nutzen und Schaden sollte die absolute Risikoreduktion verwendet werden (und nicht die relative), wie es oben beschrieben wurde.
- Für Darstellungen von Nutzen und Risiken sollen, wenn möglich, einheitliche Bezugsgrößen gewählt werden. Als Ausgangspunkt sollte ein Basisrisiko herangezogen werden (zum Beispiel der „natürliche Krankheitsverlauf“). Damit ist die Wahrscheinlichkeit gemeint, mit der sich eine Erkrankung auch ohne medizinische Intervention verbessert, verschlechtert oder konstant bleibt. Das Heranziehen einer sinnvollen Bezugsgröße (z.B. X von 100) ermöglicht es, die Effektivität einer Maßnahme besser einschätzen zu können.
- Zur Vermittlung von Zahlen und Risikoangaben werden zusätzlich graphische bzw. visuelle Darstellungen von Zahlen in Piktogrammen, Balkendiagrammen oder Tortendiagrammen empfohlen (siehe z.B. Abbildung 3).

Lösungen
Mit zunehmender Prävalenz steigt bei gleichbleibender Sensitivität und Spezifität die positive Korrektheit (s. Abbildung 4).
Darstellung eines Baums mit natürlichen Häufigkeiten zur Veranschaulichung des Nutzens von Mammographiescreenings (s. Abbildung 5)
4.3.3. Beteiligung an medizinischen Entscheidungen
Da Patientenbedürfnisse zunehmend in den Mittelpunkt einer qualitativ hochwertigen Versorgung rücken und zudem ein eigenverantwortlicher Umgang von Patienten mit ihrer Erkrankung gefordert wird, hat eine patientenzentrierte Gesundheitsversorgung in den letzten Jahren mehr und mehr an Bedeutung gewonnen. Basierend auf einer systematischen Zusammenfassung der in der wissenschaftlichen Literatur beschriebenen Definitionen benennt ein integratives Modell insgesamt 15 relevante Dimensionen einer patientenzentrierten Gesundheitsversorgung [15], die in drei übergeordnete Kategorien (Grundprinzipien, förderliche Faktoren, Handlungen und Maßnahmen) unterteilt werden können (siehe Tabelle 4).
|
Grundprinzipien |
|
|
Grundlegende Eigenschaften des Behandlers |
Einstellungen gegenüber dem Patienten (z.B. Empathie, Respekt, Ehrlichkeit) und sich selbst gegenüber (Selbstreflexion) |
|
Behandler-Patient-Beziehung |
Eine durch Vertrauen und Fürsorge geprägte Beziehung zum Patienten (therapeutische Allianz) |
|
Patient als Individuum |
Anerkennung der Einzigartigkeit des Patienten (Gefühle, Ansichten, Anliegen, individuelle Bedürfnisse, Erwartungen und Präferenzen) |
|
Förderliche Faktoren |
|
|
Behandler-Patienten-Kommunikation |
Professionelle verbale und nonverbale Kommunikationsfertigkeiten, die adäquat eingesetzt werden |
|
Integration medizinischer und nicht-medizinischer Versorgung |
Anerkennung der Relevanz und Integration nicht-medizinischer Aspekte der Versorgung (z.B. Selbsthilfe) in die Behandlung |
|
Zusammenarbeit und Teamentwicklung |
Anerkennung und Förderung effektiver Teams, die sich durch Respekt, Vertrauen, gemeinsame Verantwortung und Werte auszeichnen |
|
Zugang zur Versorgung |
Gewährleistung eines adäquaten und auf Bedürfnisse der Patienten zugeschnittenen Zugangs (z.B. zur ambulanten Psychoonkologie) |
|
Koordination und Kontinuität der Versorgung |
Förderung einer gut koordinierten Versorgung (z.B. bzgl. Folgeuntersuchung) und Kontinuität (stationäre und ambulante Behandlung) |
|
Handlungen / Maßnahmen |
|
|
Patienteninformation |
Vermittlung und Bereitstellung von Informationen unter Berücksichtigung der Informationsbedürfnisse und -präferenzen des Patienten |
|
Patientenbeteiligung an Versorgungsprozessen |
Aktive Zusammenarbeit und aktive Beteiligung unter Berücksichtigung der Beteiligungspräferenzen des Patienten |
|
Beteiligung von Familienangehörigen und Freunden |
Aktive Beteiligung und Unterstützung der Verwandten und Freunde des Patienten in dem Maße, wie Patienten es wünschen |
|
Empowerment des Patienten |
Anerkennung und aktive Unterstützung der Fähigkeiten und Verantwortung des Patienten zum Selbstmanagement seiner Krankheit |
|
Physische Unterstützung |
Maßnahmen, die die Unterstützung des Patienten auf körperlicher Ebene gewährleisten (z.B. Schmerz- oder Physiotherapie) |
|
Emotionale Unterstützung |
Wahrnehmen der emotionalen Situation des Patienten und Eingehen auf diese; psychologische Unterstützung ermöglichen, wenn gewünscht |
Die Umsetzung einer patientenzentrierten Versorgung findet entsprechend dem integrativen Modell auf unterschiedlichen Ebenen statt: Auf der übergeordneten Ebene (Makroebene) wurden Rechte geschaffen, durch welche die Partizipation von Patienten verbessert werden soll (z.B. Patientenrechtegesetz 2013 [4]). Auf der mittleren Ebene (Mesoebene) der Institutionen im Gesundheitswesen wurden durch die Förderung der Patientenberatung sowie von Patienteninitiativen und Selbsthilfegruppen bereits etablierte Einrichtungen weiter ausgebaut bzw. neu gegründet. Die Mikroebene umfasst die individuelle medizinische Entscheidung im direkten Gespräch zwischen Arzt und Patient. In diesem Bereich ist der Ansatz des Shared Decision Making (deutsche Übersetzung: Partizipative Entscheidungsfindung - PEF) entstanden. Als Grundlage wird eine partnerschaftliche Arzt-Patient-Beziehung (Arzt-Patient-Interaktion) formuliert, die gekennzeichnet ist durch einen gemeinsamen und gleichberechtigten Entscheidungsfindungsprozess. Dieser mündet in der Auswahl von individuell auf den Patienten und dessen Bedürfnisse abgestimmten diagnostischen, therapeutischen oder weiteren gesundheitsbezogenen Maßnahmen.
4.3.3.1. Entscheidungsmodelle in der Medizin
Das Modell der partizipativen Entscheidungsfindung wird häufig in Abgrenzung zu den beiden anderen Modellen der medizinischen Entscheidungsfindung beschrieben, die in Kapitel 4.2. dargestellt wurden (paternalistisches Modell und Informationsmodell). Dabei nimmt es eine Mittelstellung zwischen diesen Modellen ein. Beim Ansatz der PEF sollen der Informationsaustausch und die Entscheidungsprozesse zwischen Arzt und Patient auf gleichberechtigter Ebene stattfinden und schließen dabei auch individuelle Aspekte wie Werte, Bedürfnisse und Emotionen des Patienten ein. PEF ist vom Konzept des informed consent abzugrenzen, in welchem zwar ähnliche Voraussetzungen (mehrere gleichwertige Behandlungsoptionen) vorliegen und ein ähnliches Ziel verfolgt wird (Stärkung der Kontrolle über die eigene gesundheitliche Versorgung), jedoch weniger aus ethischer, sondern eher aus rechtlicher Perspektive (z.B. Einwilligung zur Teilnahme an Studien, Einwilligung für eine bestimmte Behandlung).
Definiert wird PEF als Interaktionsprozess mit dem Ziel, unter gleichberechtigter aktiver Beteiligung von Patient und Arzt auf Basis geteilter Informationen zu einer gemeinsam verantworteten Übereinkunft zu kommen. Dabei fließt die Information in beide Richtungen, der Arzt stellt medizinische Informationen bereit, der Patient bezieht seine Präferenzen und persönlichen Lebensumstände mit ein, die für die Entscheidung von Relevanz sein können. Arzt und Patient treffen schließlich eine gemeinsame Entscheidung und teilen sich die Verantwortung. Dieses Modell kann auch durch andere bei medizinischen Entscheidungen beteiligte Berufsgruppen angewendet werden, z.B. durch Psychologen in der psychotherapeutischen Versorgung, die mit Patienten Entscheidungen nach Diskussion verschiedener Behandlungsmöglichkeiten bei psychischen Erkrankungen vorbereiten.
4.3.3.2. Umsetzung in der Arzt-Patient-Kommunikation
Die Umsetzung einer partizipativen Entscheidungsfindung folgt einem klar erkennbaren Ablauf mit aufeinander aufbauenden Handlungsschritten, wobei Informationen in mindestens zwei Richtungen fließen. Ärzte stellen notwendige medizinische Informationen bereit, Patienten berichten von ihren Präferenzen und persönlichen Lebensumständen (Werte, Bedürfnisse, Ziele), die für die gesundheitsbezogene Entscheidung von Relevanz sein können. Für eine gelungene Partizipation an einer medizinischen Entscheidung wurden folgende konsensuell entwickelte Handlungsschritte (s. Abbildung 6) vorgelegt [16]: Der gemeinsame Entscheidungsprozess beginnt, indem zunächst von ärztlicher Seite die Notwendigkeit einer Behandlungsentscheidung und das Angebot einer gleichberechtigten Zusammenarbeit beider Partner bei der Entscheidungsfindung formuliert werden. Wenn der Patient auf das Angebot eingeht, d.h. explizit eine partizipative Entscheidungsfindung wünscht (s. die Ausführungen in Kapitel 4.2., denen zufolge dies nicht immer der Fall ist), erfolgt im nächsten Schritt die Beschreibung der unterschiedlichen Behandlungsmöglichkeiten mit ihren jeweiligen Vor- und Nachteilen. Anschließend wird der Patient zu seinem Verständnis der Informationen sowie nach seinen Erwartungen und Befürchtungen hinsichtlich der Entscheidung befragt. Im nächsten Schritt werden die unterschiedlichen Präferenzen von Patient und Arzt ermittelt, ein Abwägen der Behandlungsalternativen erfolgt und ein Plan zur Umsetzung der gewählten Behandlung wird beschlossen.
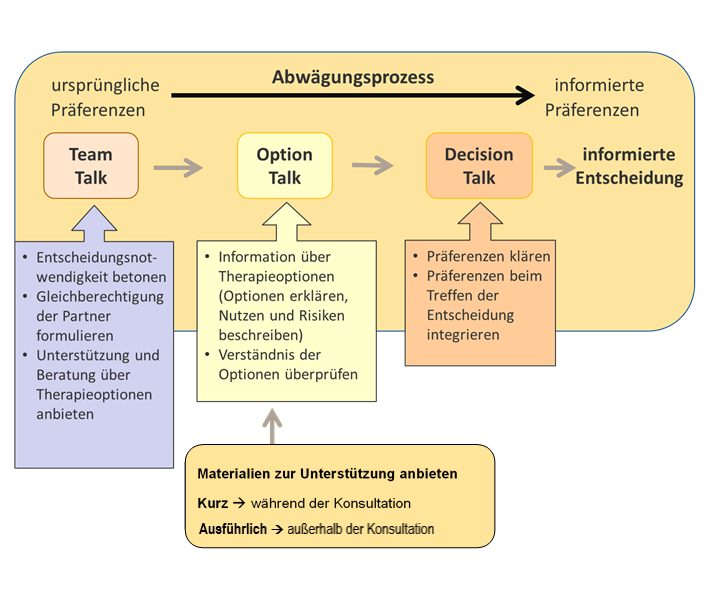
Das Konzept der partizipativen Entscheidungsfindung ist insbesondere in Situationen medizinischer Unsicherheit angezeigt. Unsicherheit kann bei sogenannten präferenzsensitiven Entscheidungen eine Rolle spielen, wenn die medizinische Evidenz und klinische Erfahrung mehr als eine Behandlungsoption ermöglichen und wenn die Wahl von den persönlichen Präferenzen, Charakteristika und Umständen der Patienten beeinflusst wird. Unsicherheit kann auch eine Rolle spielen, wenn die wissenschaftliche Evidenz nicht eindeutig oder nicht vorhanden ist. Außerdem ist PEF geeignet, wenn die Wichtigkeit der Entscheidung und der Konsequenzen für den Patienten hoch ist, d. h., wenn es sich um eine chronische und lebensverändernde Erkrankung handelt. PEF sollte in dem Ausmaß stattfinden, das von Patienten in der jeweiligen Situation tatsächlich gewünscht wird. In Krisen- oder Notfallsituationen oder wenn sich Patienten durch eine Beteiligung überfordert fühlen, ist PEF weniger oder gar nicht angebracht.
4.3.3.3. Evidenzbasierte Gesundheitsinformationen und medizinische Entscheidungshilfen
Eine evidenzbasierte Gesundheitsinformation soll dabei unterstützen, eine Behandlung entsprechend der individuellen Präferenzen des Patienten zu gestalten und dabei möglichen Schaden durch Über-, Unter- oder Fehlbehandlung gering zu halten. Die Gute Praxis der Gesundheitsinformation (GPGI) (Deutsches Netzwerk Evidenzbasierte Medizin 2015 [18]) legt Kriterien im Hinblick auf Verständlichkeit und Transparenz der Inhalte von evidenzbasierten Gesundheitsinformationen fest. Dadurch soll es Patienten und auch Behandlern erleichtert werden, medizinische Inhalte auf relevante Qualitätsanforderungen zu überprüfen. Qualitätsgeprüfte evidenzbasierte Gesundheitsinformationen vermitteln v.a. folgende Inhalte:
- allgemeines Wissen über Gesundheit, Erkrankungen, ihre Auswirkungen und ihren Verlauf,
- Maßnahmen zur Gesunderhaltung (Prävention und Gesundheitsförderung),
- Früherkennung, Diagnostik, Behandlung, Rehabilitation und Nachsorge von Krankheiten und damit im Zusammenhang stehenden medizinischen Entscheidungen,
- Pflege, Krankheitsbewältigung und den Alltag mit einer Erkrankung.
Informationen zur Abwägung von Nutzen und Risiken einer medizinischen Behandlung sowie über die patientenrelevanten Ergebnisse sollen in Gesundheitsinformationen im Vergleich zu einer Scheinbehandlung (zum Beispiel Placebo) oder zu einer anderen Behandlungsoption präsentiert werden. Verlässliche und evidenzbasierte Gesundheitsinformationen werden inzwischen von mehreren seriösen Anbietern im Gesundheitswesen bereitgehalten. Besonders wichtig sind die entstandenen Bibliotheken des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG), hier die Webseite www.gesundheitsinformation.de, und die Bibliothek zu Patienteninformationen, auch mehrsprachig, des Ärztlichen Zentrums für Qualität in der Medizin (ÄZQ) unter www.patienten-information.de.
Medizinische Entscheidungshilfen beinhalten standardisierte Informationen, eine verständliche Darstellung von Behandlungsmöglichkeiten und der jeweiligen Vor- und Nachteile sowie Wahrscheinlichkeiten für einen Behandlungserfolg. Zudem werden Werte und Präferenzen auf Seiten der Patienten im Rahmen der Entscheidungsfindung berücksichtigt und integriert. Entscheidungshilfen (sogenannte decision aids) können dem Patienten text-, video- oder webbasiert dargeboten werden. In den letzten Jahren werden Entscheidungshilfen zunehmend webbasiert umgesetzt, zudem werden mittlerweile auch stark komprimierte Entscheidungshilfen erarbeitet. Diese enthalten Zusammenfassungen der wichtigsten Wirkungen und Nebeneffekte von diagnostischen und therapeutischen Maßnahmen bzw. bewerten die jeweils wichtigsten Fragen bezüglich verschiedener Behandlungsoptionen mit Vor- und Nachteilen. Beispiele sind Entscheidungshilfen zu psychischen Erkrankungen (z.B. Depressionen, Angststörungen, Rückkehr zur Arbeit, Psychosen), wie sie auf der Plattform „psychenet – Netz psychische Gesundheit“ (s. Link) angeboten werden oder für die Entscheidung hinsichtlich Vorsorgemaßnahmen, z.B. Mammographie (s. Link), PSA-Screening für Prostatakrebs (s. Link), bereitgehalten werden.
Eine Zusammenfassung von bisher durchgeführten Studien im Rahmen eines Cochrane-Reviews belegte, dass der Einsatz von Entscheidungshilfen zu mehr Wissen, realistischeren Erwartungen über den Erkrankungsverlauf, höherer Zufriedenheit und verbesserter Therapietreue führt. Zudem resultierten eine Reduktion von Entscheidungskonflikten und eine stärker erlebte Beteiligung an Behandlungsentscheidungen [19].
4.3.4. Kommunikation zur Verhaltensmodifikation
Neben dem Ansatz der partizipativen Entscheidungsfindung existieren weitere Ansätze, die eine Partizipation an der Gesundheitsversorgung auf Seiten des Patienten fokussieren. Eine aktive Beteiligung von Patienten an der Behandlung ihrer chronischen Erkrankung ist beispielsweise explizit im Rahmen des sogenannten Chronic-Care-Modells verankert (deutsche Adaptation siehe [20]). Neben dem Einsatz evidenzbasierter fachspezifischer Leitlinien, also Empfehlungen zum diagnostischen und therapeutischen Vorgehen (vgl. Kapitel 3.4.4.), strukturierten Arbeitsabläufen, Vernetzung der Versorgungseinrichtung und dem Einsatz klinischer Informationssysteme (z.B. elektronische Patientenakte und vereinfachte Kommunikationswege von Behandlungseinrichtungen) soll insbesondere über ein verbessertes Selbstmanagement die aktive Rolle des Patienten im Behandlungsverlauf gestärkt werden (vgl. Kapitel 3.2.2.). Unter Selbstmanagement wird in diesem Zusammenhang die Hilfe zur Selbsthilfe verstanden, um eine Stärkung der Patientenrolle und -kompetenz zu erreichen und Patienten zu motivieren, selbstständig Ziele zu setzen, Barrieren und Herausforderungen zu identifizieren und den Gesundheitszustand zu überwachen [20]. Selbstmanagement von chronischen Erkrankungen bezieht sich dabei insbesondere auf Bereiche wie adäquaten Medikamentengebrauch (regelmäßig, kontrolliert), sinnvolle und machbare Lebensstilveränderungen zur Risikofaktorenminderung (z.B. Rauchstopp, Ernährungsumstellung), angemessene Verhaltensänderungen zur Prävention von Langzeitkomplikationen (regelmäßige Bewegungseinheiten) oder die Adhärenz bezüglich der vereinbarten Behandlungspläne.
4.3.4.1. Motivierende Gesprächsführung
Um Verhaltensänderungen bei Patienten herbeizuführen, können spezifische Gesprächstechniken eingesetzt werden, die sich hierzu besonders gut eignen. Speziell bei Indikationen wie Nikotin- oder Alkoholkonsum ist das sogenannte Motivational Interviewing (= motivierende Gesprächsführung) eine besonders geeignete Technik. Das Konzept wurde ursprünglich zur Beratung für Menschen mit Suchtproblemen entwickelt [21] und ist ein klientenzentrierter Beratungsansatz (vgl. Kapitel 4.2.), mit dem Ziel, eine stabile innere (= intrinsische) Motivation zur Verhaltensänderung aufzubauen. Es nutzt auch aktivere, kognitiv-behaviorale Strategien, die direktiv auf ein Zielverhalten, z.B. Nichtrauchen, (im Sinne des transtheoretischen Modells, vgl. Kapitel 5.1.) ausgerichtet sind. Motivational Interviewing (MI) kommt vorrangig zur Anwendung, um die Ambivalenz von Patienten bzw. deren Barrieren bezüglich notwendiger Verhaltensänderungen (z.B. zur Umsetzung eines gesundheitsförderlichen Lebensstils oder zur Steigerung der Medikamentenadhärenz) zu verringern und sie dabei zu unterstützen, relevante Verhaltensänderungen leichter umsetzen zu können (z.B. mit dem Rauchen aufzuhören). Bei der Anwendung von MI geht es also nicht darum, Verhaltensänderungen durchsetzen zu wollen, die vom Patienten nicht akzeptiert werden. Grundlegendes Ziel von MI ist, die Adhärenz bezüglich Empfehlungen zu Verhaltensänderungen zu erhöhen. Zu Beginn ist es notwendig, Ambivalenzen hinsichtlich der Verhaltensänderung herauszuarbeiten, um so bestehende kognitive Dissonanzen zu verstärken. Kognitive Dissonanz bezeichnet einen als unangenehm empfundenen Gefühlszustand, der dadurch entsteht, dass die eigenen Handlungen (bzw. die Art, wie man diese selbst wahrnimmt) mit den eigenen Kognitionen, also Gedanken, Einstellungen, Wünschen oder Absichten, nicht übereinstimmen. Diese Dissonanz erzeugt eine innere Spannung, der Mensch befindet sich im Ungleichgewicht und ist bestrebt, wieder einen konsistenten Zustand – ein Gleichgewicht – zu erreichen, die bestehende Dissonanz also abzubauen. Hierzu ein Beispiel: Bezüglich des Rauchens wissen die meisten Patienten, dass es gesünder wäre und Geld sparen würde, mit dem Rauchen aufzuhören – damit liegt eine kognitive Dissonanz vor. Oft versuchen die Betroffenen dann eine Dissonanzreduktion durch (Schein-)Argumente zu erreichen: „Das Rauchen entspannt mich schließlich auch und sorgt für mehr soziale Kontakte.“)
Nachdem die kognitiven Dissonanzen herausgearbeitet und damit wieder verstärkt wurden, werden die positiven und negativen Aspekte der Verhaltensänderung exploriert und besprochen, um eine tragfähige Motivation für eine Verhaltensänderung zu schaffen. Grundlegende Zielsetzungen von MI sind:
- Förderung der Änderungsmotivation: Dieses Ziel soll erreicht werden, indem der Abwägungsprozess zwischen Nutzen und Kosten einer (Verhaltens-) Änderung intensiviert wird. Dadurch soll erreicht werden, dass den Gründen für eine Veränderung mehr Gewicht verliehen wird.
- Festlegung von Zielen und konkreten Änderungsplänen: In dieser Phase sollen dann für ein konkretes Anliegen die Ziele für die Verhaltensänderung festgelegt und mittels geeigneter, geplanter Mittel umgesetzt werden.
Um diese beiden übergeordneten Zielsetzungen verwirklichen zu können, wendet MI vier Grundprinzipien an:
a) Empathie ausdrücken: Hiermit ist gemeint, dem Patienten respektvoll zuzuhören, ihn anzunehmen, wie er ist, und sein Erleben und Verhalten aus der Perspektive des Patienten zu verstehen und zu akzeptieren sowie dies dem Patienten auch zu vermitteln. Beispiele für die Gesprächsführung:
- „Sie haben einen großen Schritt getan, indem Sie sich zur Teilnahme an diesen Treffen bereit erklärt haben, vielen Dank.“
- „Ich würde gerne mit Ihnen über das Rauchen sprechen. Wie sieht denn ein normaler Tag bei Ihnen aus? Und welche Rolle spielt das Rauchen in Ihrem Tagesablauf?“
b) Diskrepanzen entwickeln: Dabei steht im Vordergrund, gemeinsam mit dem Patienten herauszuarbeiten, wie das problematische Verhalten mit grundlegenden Zielen des Patienten in Konflikt steht, z.B. indem über Nachteile des zu ändernden Verhaltens gesprochen wird, bzw. über die Vorteile, wenn Änderungen stattgefunden haben. Beispiel:
- „Sie stellen fest, dass ein Unterschied besteht zwischen Ihrer jetzigen Situation und dem, was Sie sich vom Leben wünschen würden.“
c) Hilfreicher Umgang mit Widerstand: Eine wesentliche Komponente des MI ist, auf Widerstände von Seiten des Patienten bezüglich der Verhaltensänderungen nicht mit verstärkter Überzeugungsarbeit zu reagieren, sondern zu versuchen, diese Widerstände wertzuschätzen und sie als „normales Verhalten“ zu verstehen. Beispiele:
- „Auf der einen Seite hat Ihnen das Rauchen einige Probleme bereitet, auf der anderen Seite wollen Sie keine Unterstützung erhalten, wie passt das zusammen?“
- „Sie haben Recht. Ohne einen Plan, wie Sie künftig mit beruflichen Belastungen besser umgehen, macht es wahrscheinlich keinen Sinn, über eine Veränderung des Rauchverhaltens nachzudenken. Was meinen Sie dazu?“
d) Änderungszuversicht stärken: Ein weiterer zentraler Aspekt des MI ist die Arbeit an der Selbstwirksamkeit des Patienten (s. auch Kapitel 3.2.1. und 5.1.), z.B. indem auf Erfolge bei früheren Verhaltensänderungen Bezug genommen wird. Beispiele:
- „Sie haben es letzte Woche geschafft, das Rauchen deutlich zu reduzieren, darauf können Sie stolz sein. Wie sehen Sie dies selbst?“
- „Wie wollen Sie nun selbst weitermachen? Wie kann ich Sie dabei weiter unterstützen, damit Sie Ihre Ziele erreichen?“
Obwohl ursprünglich für den Suchtbereich entwickelt, belegen verschiedene Zusammenfassungen von Studien im Rahmen von Meta-Analysen, dass MI auch bei weiteren Indikationsbereichen erfolgreich eingesetzt werden kann, z.B. bezüglich Medikamentenadhärenz [22], [23], Steigerung der körperlichen Aktivität [24] bzw. weiterer gesundheitsverhaltensbezogener Ergebnisparameter, wie z.B. Ernährung, Gewichtsreduktion [25], [26].
4.3.4.2. Zielsetzung und -erreichung
Eine weitere Strategie zur Umsetzung von Verhaltensänderungen im Sinne eines verbesserten Selbstmanagements stellen Zielvereinbarungen (engl. goal setting) dar. Unter einer Zielvereinbarung wird ein Prozess verstanden, in welchem Behandler und Patient sich gemeinsam auf gesundheitsbezogene Zielsetzungen einigen. Durch adäquat formulierte Zielsetzungen wird die Motivation, diese Ziele tatsächlich umzusetzen, und somit auch die Zielerreichung, positiv beeinflusst [27].
Adäquate Formulierungen von Zielen zeichnen sich dadurch aus, dass sie von der Person selbst ausgewählt werden, die Zielerreichung einen hohen Anreiz darstellt (Wünschbarkeit), gleichzeitig aber machbar erscheint (Machbarkeit), die Person sich also als ausreichend kompetent erlebt, um zielgerichtetes Handeln erfolgreich auszuführen. Zudem sollten Ziele möglichst konkret und positiv formuliert werden [27] und im Sinne des mentalen Kontrastierens sowohl positive Effekte der Zielerreichung wie auch hinderliche Faktoren berücksichtigen [28].
Hilfreich für die Zielformulierung können Vorgaben wie z.B. die S.M.A.R.T.-Regel sein:
S = spezifisch (specific): Spezifische, konkrete Ziele haben einen höheren Einfluss auf die Motivation zur Zielerreichung als unklar formulierte Ziele.
M = messbar (measurable): Ein Ziel sollte so formuliert werden, dass am Ende objektiv beurteilt werden kann, ob es erreicht wurde.
A = wünschenswert (attractive): Ein Ziel sollte so formuliert sein, dass es den eigenen Bedürfnissen entspricht und eine hohe Attraktivität für die Person besitzt.
R = realistisch (realistic): Die Zielsetzung sollte so formuliert sein, dass man sich in der Lage fühlt, das Ziel auch realistisch zu erreichen.
T = zeitlich begrenzt (time-phased): Die Dauer für die Zielerreichung sollte klar festgelegt sein.
Um ein bestimmtes Ziel konkret zu realisieren (engl. goal striving), sind dann im Weiteren spezifische Selbstregulationsstrategien im Sinne von Durchführungsvorsätzen (implementation intentions) hilfreich, z.B. sogenannte Wenn-Dann-Pläne [29]. Um das Ziel zu erreichen, kann es also hilfreich sein, konkrete Verhaltenspläne zu formulieren, wie z.B.: „Wenn Situation x eintritt, dann werde ich Verhalten y ausführen.“ Die Zielerreichung wird also dadurch begünstigt, dass genauer festgelegt wird, an welchem Ort, zu welcher Zeit und auf welche Art und Weise ein bestimmtes Ziel erreicht werden soll [29].
Um gesundheitsförderliche Lebensstilveränderungen (z.B. „Ich möchte meinen Zigarettenkonsum reduzieren.“) erfolgreich umzusetzen, kann es zunächst hilfreich sein, sich die positiven Konsequenzen (geringeres Risiko für verschiedene Erkrankungen), wie auch Hindernisse, die der Zielerreichung im Wege stehen (großes Verlangen nach einer Zigarette nach dem Abendessen), zu vergegenwärtigen. Darauf aufbauend können dann konkrete Durchführungsvorsätze („Immer wenn ich nach dem Abendessen das Verlangen nach einer Zigarette habe, mache ich einen kurzen Spaziergang um den Block.“) hilfreich bei der Zielerreichung sein.
4.3.4.3. Mangelnde Adhärenz
Werden Behandlungsempfehlungen nicht wie vereinbart umgesetzt, spricht man von mangelnder Adhärenz (oder auch Non-Adhärenz bzw. mangelnder Compliance/Non-Compliance). Diese kann intentional sein, also auf eine bewusste Entscheidung des Patienten zurückgehen, oder non-intentional, also versehentlich entstehen. Wenn Patienten dauerhaft Probleme mit der Umsetzung ihrer Therapieempfehlungen haben, kann das den Krankheitsverlauf ungünstig beeinflussen und den Behandlungserfolg gefährden. Infolge von Non-Adhärenz können die Belastungen durch Erkrankungen höher sein, mehr Folgeerkrankungen auftreten, oder die Erkrankung kann länger andauern. Die Umsetzung von Therapieempfehlungen ist also für eine erfolgreiche Behandlung sehr wichtig, vor allem im Bereich der chronischen Erkrankungen, wie z.B. bei Diabetes oder Herz-Kreislauf-Erkrankungen.
Die Weltgesundheitsorganisation schätzt, dass nur etwa 50% der Patienten eine gute Therapietreue aufweisen und somit ihren Therapieplan dauerhaft konsequent umsetzen. Dies trifft insbesondere auf Patienten mit chronischen Erkrankungen zu.
Die Gründe für eine unzureichende Adhärenz sind sehr individuell. Meist spielen verschiedene Faktoren eine Rolle. Hinsichtlich möglicher Ursachen von Non-Compliance werden drei Arten unterschieden [30].
- Intelligente Non-Adhärenz: Aufgrund von Nebenwirkungen, ausbleibenden Behandlungserfolgen bzw. nicht nachvollziehbaren Anordnungen bricht der Patient die Behandlung ab bzw. beginnt sie erst gar nicht.
- Adaptive Non-Adhärenz: Der Patient wägt ab, ob z.B. seine Lebensqualität mit oder ohne Behandlung höher ist, und bricht deswegen die Behandlung ab.
- Beanspruchungs-Non-Adhärenz: Der Patient bricht die Behandlung ab, da es aufgrund der aktuellen Lebensumstände (z.B. Krise) schwierig ist, diese umzusetzen.
Dabei ist wichtig, dass die Ursachen nicht nur auf Seiten des Patienten (oder der Angehörigen) liegen, sondern darüber hinaus viel mit der Arzt-Patient-Beziehung, der zugrunde liegenden Erkrankung sowie der Behandlungsempfehlung selbst zu tun haben können. Die Qualität der Kommunikation mit dem Arzt sowie eine vertrauensvolle Beziehung zu dem behandelnden Arzt haben eine zentrale Bedeutung für die erfolgreiche Umsetzung von Behandlungsempfehlungen. Es gibt auch Ursachen für eine unzureichende Adhärenz, die direkt mit der Erkrankung zusammenhängen. Wenn keine oder nur wenig Beschwerden bzw. Symptome spürbar sind (z.B. bei Bluthochdruck oder hohem Cholesterinspiegel), wird der Nutzen der Behandlungsmöglichkeit vielleicht nicht ausreichend nachvollziehbar sein, wenn dies im ärztlichen Gespräch nur unzureichend thematisiert wurde. Ebenso kann eine längerfristig eingeschränkte Stimmung (z.B. bei Depressionen) zu Adhärenzproblemen führen.
Auch die im ärztlichen Gespräch empfohlenen Behandlungsmaßnahmen selbst können sich negativ auf die Adhärenz auswirken. Als häufigste Ursachen sind dabei möglicherweise auftretende Nebenwirkungen (z.B. Übelkeit, Müdigkeit, Kopfschmerzen) und Sorgen um eine mögliche Medikamentenabhängigkeit zu nennen. Ist die Umsetzung der Behandlungsempfehlung komplex, z.B. aufgrund verschiedener Therapieemepfehlungen bei komorbid vorhandenen Erkrankungen (z.B. Hypertonie, Diabetes und erhöhte Cholesterinwerte) mit mehreren Tabletteneinnahmen zu mehreren Zeitpunkten pro Tag, kann dadurch ebenfalls die Adhärenz beeinträchtigt werden. Hier kommt es zur Unterlassung/Auslassung (z.B. aus Vergesslichkeit), zu Dosierungsfehlern (z.B. wird die falsche Dosis eingenommen oder die Krankengymnastik wird übertrieben), zu Frequenzfehlern (z.B. wird das Medikament zu häufig eingenommen oder die Krankengymnastik zu selten durchgeführt), zu einer Anwendung zur falschen Zeit (z.B. mit einer Mahlzeit statt auf nüchternen Magen, morgens statt abends) und zu Applikationsfehlern (z.B. wird das Asthmaspray ohne einzuatmen in die Mundhöhle gesprüht, die Krankengymnastik wird falsch ausgeführt). Auch eine lange Behandlungsdauer, häufige Veränderungen der Behandlungsempfehlungen oder der Dosierung können es Patienten erschweren, Therapiepläne konsequent umzusetzen. Gelegentlich nehmen Patienten auch „Arzneimittelferien“, d.h. sie setzen die Einnahme aus, z.B. weil sich die Beschwerden gebessert haben. Problematisch kann auch sein, wenn durch eine Behandlungsempfehlung nicht unmittelbar positive Effekte spürbar sind (z.B. bei der Behandlung von Bluthochdruck oder vorbeugenden Maßnahmen bei Herzerkrankungen).
Persönliche Faktoren können ebenfalls die Adhärenz beeinträchtigen: So können finanzielle Belastungen (Zuzahlungen bei Medikamenten und Arztbesuchen) hoch sein, oder die nächste Arztpraxis oder Apotheke ist nur schwer zu erreichen. Weitere Gründe sind Sprachbarrieren oder ein eher unregelmäßiger Alltag. Vor allem bei älteren Patienten können weitere Faktoren wie Einschränkungen der Sehfähigkeit, des Hörvermögens oder des Gedächtnisses hinzukommen. Ältere Menschen haben zudem möglicherweise keine ausreichende Unterstützung von Seiten der Familie oder von Freunden bei der Umsetzung von Therapiemaßnahmen, die sie alleine nicht bewältigen können.
4.3.5. Gesundheitskompetenz
Ärzte geben häufig an, dass eine partnerschaftlich geprägte Arzt-Patient-Beziehung aufgrund bestimmter Patienteneigenschaften (Bildung, Sprachkenntnisse) und bestimmter klinischer Situationen (Notfallsituation, kognitive Einschränkungen der Patienten) nicht oder nur schwer umsetzbar sei bzw. nicht den Präferenzen des Patienten entspreche. Patientenseitig wird als mögliche Barriere insbesondere eine eingeschränkte Gesundheitskompetenz diskutiert. Gesundheitskompetenz (engl. health literacy) ist definiert als das Ausmaß der Fähigkeit, grundlegende Gesundheitsinformationen und Angebote, die für angemessene gesundheitsrelevante Entscheidungen und Handlungen erforderlich sind, zu erhalten, zu verarbeiten und zu verstehen. Es werden drei aufeinander aufbauende Dimensionen von Gesundheitskompetenz unterschieden [31].
- Funktionale Dimension: Grundfertigkeiten im Lesen und Schreiben, die es beispielsweise ermöglichen, gesundheitsrelevante Informationen zu verstehen
- Interaktive/kommunikative Dimension: insbesondere soziale Fähigkeiten, wie zum Beispiel aktive Informationsbeschaffung zu Gesundheitsthemen und Kommunikation darüber; Anwendung dieser Informationen
- Kritische Dimension: Fähigkeit, sich mit gesundheitsbezogenen Informationen kritisch auseinanderzusetzen und diese im Sinne einer verbesserten Krankheitsbewältigung optimal zu nutzen
Studien zeigen, dass eine eingeschränkte Gesundheitskompetenz sich negativ auf die Arzt-Patient-Kommunikation auswirken kann [32], weswegen neue Ansätze versuchen, geringer ausgeprägte Gesundheitskompetenz stärker zu berücksichtigen [33]. Es werden verschiedene weitere Strategien diskutiert, wie Behandler die Kommunikation mit Patienten, die eine eingeschränkte Gesundheitskompetenz aufweisen, optimieren können (vgl. z.B. [34]):
Informationsgewinnung
- Aktives Zuhören einsetzen und non-verbale Kommunikation berücksichtigen
- Offene Fragen verwenden und Patienten ermutigen, selbst Fragen zu stellen
- Dem Patienten die Möglichkeit geben, einen Angehörigen oder andere Vertrauenspersonen hinzuzuziehen
- Wissensstand des Patienten bezüglich seiner gesundheitlichen Belange/seines Gesundheitsproblems abfragen, ohne den Patienten dadurch einzuschüchtern
Informationsvermittlung
- Nur wenige Informationen auf einmal vermitteln, Reduktion des Informationsgehalts auf die relevanten Aspekte
- Verlangsamung der Sprechgeschwindigkeit, Verwenden einfacher, klarer, laiengerechter Sprache, keine Verwendung medizinischer Fachbegriffe und Abkürzungen
- Verwendung von visuellen Hilfsmitteln (z.B. Abbildungen, Zeichnungen) im Gespräch; Verwendung von handlungsorientierten Aussagen, damit Patienten wissen, was sie tun müssen
- Informationsvermittlung interaktiv gestalten, um Verarbeitung und Erinnerung positiv zu beeinflussen
- Wiederholung der vermittelten Information durch den Arzt; Patienten bitten, die vermittelten Information selbst zu wiederholen (= Teach-Back); Patienten beim nächsten Termin oder zwischenzeitlichen Telefonat fragen, ob alles verstanden wurde bzw. umgesetzt werden konnte
- Relevante Informationen schriftlich festhalten bzw. gedruckte Informationsbroschüren mitgeben; wichtige Aspekte in Informationsbroschüren kennzeichnen
- Verwendung von Risikokommunikationsstrategien, die an das individuelle Niveau des Patienten angepasst sind
Es ist allerdings noch unklar, welche dieser genannten Aspekte am relevantesten sind bzw. den größten Effekt auf die Gesundheitskompetenz der Patienten haben.
4.3.6. Zusammenfassung
Die Umsetzung einer dem Behandlungsprozess förderlichen Arzt-Patient-Beziehung ist ein zentraler Aspekt im Rahmen einer patientenzentrierten, erfolgreichen Gesundheitsversorgung. Relevante Aspekte einer erfolgreichen Arzt-Patient-Kommunikation beziehen sich sowohl auf die Art und Weise der Diagnosemitteilung, eine für Patienten angemessene Aufklärung, die Behandlungsauswahl und -planung sowie die Besprechung gesundheitsbezogener Verhaltensänderungen. Durch eine professionelle und der Situation angemessene Arzt-Patient-Kommunikation kann die Zufriedenheit mit der ärztlichen Konsultation wie auch die Adhärenz mit Behandlungsempfehlungen auf effektive Weise positiv beeinflusst werden.
1 Mit einer Vorsorgevollmacht bevollmächtigt eine Person eine andere Person, im Falle einer Notsituation alle oder bestimmte Aufgaben für den Vollmachtgeber zu erledigen. Mit der Vorsorgevollmacht wird der Bevollmächtigte zum Vertreter im Willen, d. h. er entscheidet an Stelle des nicht mehr entscheidungsfähigen Vollmachtgebers.
References
[1] Chewning B, Bylund CL, Shah B, Arora NK, Gueguen JA, Makoul G. Patient preferences for shared decisions: a systematic review. Patient Educ Couns. 2012;86(1):9-18. DOI: 10.1016/j.pec.2011.02.004[2] Silverman J, Kurtz SM, Draper,J. Skills for communicating with patients. London, New York: Radcliffe Publishing; 2013.
[3] Smith R. Patient-centered interviewing: an evidence-based method. Philadelphia: Lippincott-Williams & Wilkins; 2002.
[4] Bundesgesetzblatt (2013). Teil I Nr. 9, ausgegeben zu Bonn am 25. Februar 2013 (Gesetz zur Verbesserung der Rechte von Patientinnen und Patienten, § 630d-e, BGB).
[5] Bundesgesetzblatt (2013). Teil I Nr. 9, ausgegeben zu Bonn am 25. Februar 2013 (Gesetz zur Verbesserung der Rechte von Patientinnen und Patienten, § 630a, BGB).
[6] Schulz von Thun F. Miteinander Reden 1: Störungen und Klärungen. Reinbek bei Hamburg: Rowohlt; 1981.
[7] Bundesärztekammer. (Muster-)Berufsordnung für die in Deutschland tätigen Ärztinnen und Ärzte – MBO-Ä 1997 –* in der Fassung des Beschlusses des 121. Deutschen Ärztetages 2018 in Erfurt. Dtsch Arztebl. 2019;116(5): A-230 / B-194 / C-194.
[8] Faller H, Lang H. Medizinische Psychologie und medizinische Soziologie. Heidelberg: Springer Medizin-Verlag; 2010.
[9] Langewitz W. Arzt-Patient-Kommunikation, Mitteilen schlechter Nachrichten. In: Handlungsfelder der Psychosozialen Medizin. Brähler E, Strauß B, editors. Göttingen: Hogrefe; 2002. p. 54-76.
[10] Wiesing U, Bürger ME, Faul C, Garmer H, Göth M, Kamps H, et al. Die Aufklärung von Tumorpatienten – Informationen und Empfehlungen für das betreuende Team. Tübingen: Südwestdeutsches Tumorzentrum – Comprehensive Cancer Center Tübingen; 2008. DOI: 10.4126/38m-002617516
[11] Baile WF, Buckman R, Lenzi R, Glober G, Beale EA, Kudelka AP. SPIKES - A six-step protocol for delivering bad news: application to the patient with cancer. Oncologist. 2000;5(4):302-11. DOI: 10.1634/theoncologist.5-4-302
[12] Gigerenzer G. Das Einmaleins der Skepsis - Über den richtigen Umgang mit Zahlen und Risiken. München/Berlin: Piper Verlag; 2015.
[13] Gemeinsamer Bundesausschuss. MAMMOGRAPHIE-SCREENING – Eine Entscheidungshilfe. Programm zur Früherkennungvon Brustkrebs für Frauenzwischen 50 und 69 Jahren. 2017 [cited 2020 May 12]. Available from: https://www.mammo-programm.de/download/downloads/broschueren/2017-08-23_G-BA_Entscheidungshilfe_Mammographie_bf.pdf#page=1
[14] Hoffmann TC, Del Mar C. Clinicians' expectations of the benefits and harms of treatments, screening, and tests: a systematic review. JAMA Intern Med. 2017;177(3):407-19. DOI: 10.1001/jamainternmed.2016.8254
[15] Scholl I, Zill JM, Härter M, Dirmaier J. An integrative model of patient-centeredness - a systematic review and concept analysis. PLoS One. 2014;9(9):e107828. Published 2014 Sep 17. DOI: 10.1371/journal.pone.0107828
[16] Elwyn G, Durand MA, Song J, Aarts J, Barr PJ, Berger Z, et al. A three-talk model for shared decision making: multistage consultation process. BMJ. 2017;359:j4891. Published 2017 Nov 6. DOI: 10.1136/bmj.j4891
[17] Härter M. Partizipative Entscheidungsfindung (Shared Decision Making)- Ein von Patienten, Ärzten und der Gesundheitspolitik geforderter Ansatz setzt sich durch [Shared decision making - from the point of view of patients, physicians and health politics is set in place]. Z Arztl Fortbild Qualitatssich. 2004;98(2):89-92.
[18] Deutsches Netzwerk Evidenzbasierte Medizin. Gute Praxis Gesundheitsinformation [Internet]. Berlin: Deutsches Netzwerk Evidenzbasierte Medizin e.V; 2015 [cited 2017 Apr 6]. Available from: http://www.ebm-netzwerk.de/gpgi
[19] Stacey D, Légaré F, Col NF, et al. Decision aids for people facing health treatment or screening decisions. Cochrane Database Syst Rev. 2014;(1):CD001431. Published 2014 Jan 28. DOI: 10.1002/14651858.CD001431.pub4
[20] Gensichen J, Muth C, Butzlaff M, Rosemann T, Raspe H, Müller de Cornejo G, et al. Die Zukunft ist chronisch: Das Chronic Care-Modell in der deutschen Primärversorgung - Übergreifende Behandlungsprinzipien einer proaktiven Versorgung für chronische Kranke [The future is chronic: German primary care and the Chronic Care Model - The comprehensive principles in the proactive treatment of the chronically ill]. Z Arztl Fortbild Qualitatssich. 2006;100(5):365-74.
[21] Miller WR, Rollnick S. Motivational interviewing: Preparing people to change addictive behavior. New York: Guilford Press; 1999.
[22] Palacio A, Garay D, Langer B, Taylor J, Wood BA, Tamariz L. Motivational interviewing improves medication adherence: a systematic review and meta-analysis. J Gen Intern Med. 2016;31(8):929-40. DOI: 10.1007/s11606-016-3685-3
[23] Zomahoun HTV, Guénette L, Grégoire JP, Lauzier S, Lawani AM, Ferdynus C, et al. Effectiveness of motivational interviewing interventions on medication adherence in adults with chronic diseases: a systematic review and meta-analysis. Int J Epidemiol. 2017;46(2):589-602. DOI: 10.1093/ije/dyw273
[24] O'Halloran PD, Blackstock F, Shields N, Holland A, Iles R, Kingsley M, et al. Motivational interviewing to increase physical activity in people with chronic health conditions: a systematic review and meta-analysis. Clin Rehabil. 2014;28(12):1159-1171. DOI: 10.1177/0269215514536210
[25] Lundahl B, Moleni T, Burke BL, Butters R, Tollefson D, Butler C, et al. Motivational interviewing in medical care settings: a systematic review and meta-analysis of randomized controlled trials. Patient Educ Couns. 2013;93(2):157-68. DOI: 10.1016/j.pec.2013.07.012
[26] VanBuskirk KA, Wetherell JL. Motivational interviewing with primary care populations: a systematic review and meta-analysis. J Behav Med. 2014;37(4):768-780. DOI: 10.1007/s10865-013-9527-4
[27] Locke EA, Latham GP. Building a practically useful theory of goal setting and task motivation: a 35-year odyssey. Am Psychol. 2002;57(9):705-717. DOI: 10.1037//0003-066x.57.9.705
[28] Oettingen G, Pak H, Schnetter K. Self-regulation of goal setting: turning free fantasies about the future into binding goals. J Pers Soc Psychol. 2001;80(5):736-753. DOI: 10.1037/0022-3514.80.5.736
[29] Gollwitzer PM. Implementation intentions: strong effects of simple plans. American Psychologist. 1999;54(7):493-503. DOI: 10.1037/0003-066X.54.7.493
[30] Raspe H. Die therapeutische Kooperation von Arzt und Patient. Fortschritte der Medizin. 1980;92:1185-6.
[31] Nutbeam D. Health literacy as a public health goal: a challenge for contemporary health education and communication strategies into the 21st century. Health Promot Int. 2000;15(3):259-267. DOI: 10.1093/heapro/15.3.259
[32] Kripalani S, Jacobson TA, Mugalla IC, Cawthon CR, Niesner KJ, Vaccarino V. Health literacy and the quality of physician-patient communication during hospitalization. J Hosp Med. 2010;5(5):269-75. DOI: 10.1002/jhm.667
[33] McCaffery KJ, Smith SK, Wolf M. The challenge of shared decision making among patients with lower literacy: a framework for research and development. Med Decis Making. 2010;30(1):35-44. DOI: 10.1177/0272989X09342279
[34] Batterham RW, Hawkins M, Collins PA, Buchbinder R, Osborne RH. Health literacy: applying current concepts to improve health services and reduce health inequalities. Public Health. 2016;132:3-12. DOI: 10.1016/j.puhe.2016.01.001




